ইলেকট্রন বিন্যাসের নিয়ম
পরমাণুতে নিউক্লিয়াসের চারদিকে কতগুলো শক্তিস্তর বা সেল থাকে। ইলেক্ট্রনগুলো তাদের নিজ নিজ শক্তিস্তরে নিউক্লিয়াসকে কেন্দ্র করে অবস্থান করে। নিয়ক্লিয়াসের নিকট থেকে দূরত্ব অনুসারে শক্তিস্তরগুলোর নাম K,L,M,N,O,P ইত্যাদি।
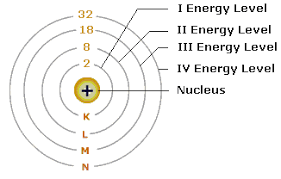
অর্থাৎ সবচেয়ে কাছে অবস্থিত ১ম শক্তিস্তর যার নাম K.এভাবে,
২য় শক্তিস্তর =L
৩য় শক্তিস্তর =M
৪র্থ শক্তিস্তর =N
৫ম শক্তিস্তর =O
-------------------------------------------------------------------
এই K,L,M,N,O,P হলো
প্রধান শক্তিস্তর।এগুলো আবার এক বা একাধিক
উপশক্তিস্তরে বিভক্ত(চিত্রে দেখানো সম্ভব নয়)।যেগুলো s,p,d,f নামে পরিচিত।
K শক্তিস্তরে থাকে1 টি উপশক্তিস্তর=s
L শক্তিস্তরে থাকে2 টি উপশক্তিস্তর=s p
M শক্তিস্তরে থাকে3 টি উপশক্তিস্তর=s p d
N শক্তিস্তরে থাকে4 টি উপশক্তিস্তর=s p d f
s p d f উপশক্তিস্তরে কপ্তগূলো অঞ্চল বা area থাকে যাদের অরবিটাল(Orbital) বলে।এই অরবিটালেই ইলেক্ট্রনগূলো অবস্থান করে
এবার
উপশক্তিস্তরগুলোর
অরবিটালসংখ্যা ভালোভাবে লক্ষ্য কর:
s উপশক্তিস্তরে থাকে 1 টি অরবিটাল
p " " 3 " "
d " " 5 " "
f " " 7 " "
খেয়াল করেছো কি অরবিটাল সংখ্যা 1, 3, 5, 7 মানে বিজোড় সংখ্যা।
প্রতিইতি উপশক্তিরের(s p d f) অরবিটালে সর্বোচ্চ 2টি ইলেক্ট্রন থাকতে পারে।প্রয়োজন আনুসারে কম হতে পারে বা নাও থাকতে পারে।
ধর H পরমাণুর ইলেক্ট্রন সংখ্যা 1 টি এখন আমরা s উপশক্তিস্তরের 1 টি তো 1 টি না রেখে 2 টি অরবিটালই পূর্ন করতে 2 টি ইলেক্ট্রন রাখতে পারি না। p d f পূরণ করা তো দূরের কথা
অরবিটাল প্রতি সর্বোচ্চ 2টি ইলেক্ট্রন রাখলে প্রতিটা উপশক্তিস্তরে সর্বোচ্চ ইলেক্ট্রন থাকতে পারবে (অরবিটাল * 2)টি।
s উপশক্তিস্তরে সর্বোচ্চ ইলেক্ট্রন থাকতে পারবে1*2=2টি
p তে থাকবে সর্বোচ্চ 3*2= 6 টি
d তে থাকবে সর্বোচ্চ 5*2= 10 টি
f তে থাকবে সর্বোচ্চ 7*2= 14 টি
এবার s=2, p=6, d=10, f=14 ধরে প্রধান শক্তিস্তরগুলোতে সর্বোচ্চ ইলেক্ট্রন থাকবে,
K=s=2 টি
L=s+p=2+6=8 টি
M=s+p+d=2+6+10=18টি
N=s+p+d+f=2+6+10+14=32টি
সূত্র: 2n2[n=1,2,3,4,5,........] তবে এটি শুধুমাত্র 1-18 টি অর্থাৎ H-Ar এর ইলেক্ট্রন বিন্যাসের ক্ষেত্রে চলে।19 no. মৌল থেকে এটি অকার্যকর।যেমন- এটি দিয়ে সঠিকভাবে Ca এর ই.বিন্যাস সম্ভব নয়।
ইলেক্ট্রনগুলো সবসময় নিম্ন শক্তিস্তর পূরণ করে উচ্চশক্তিস্তরে যাবে।যেমন-O(8)এর ইলেক্ট্রন বিন্যাসের ক্ষেত্রে প্রথম শক্তিস্তর K তে দিব 2টি এরপর L এ দিব 6 টি।মোট 8 টি হয়ে গেল।অর্থাৎ অক্সিজেনের ই.বিন্যাস 2,6
H-Ar পর্যন্ত ইলেক্ট্রন বিন্যাস তো শিখলাম।কিন্তু এরপর কি হবে?
অরবিটালে ইলেক্ট্রনগুলি শক্তির নিম্নক্রম থেকে উচ্চক্রম অনুসারে অবস্থান করে।কারন, এতে ইলেক্ট্রনগুলি স্থিতিশীলতা অর্জন করে।অরবিটাল সমূহের শক্তিক্রম নিম্নরূপ:
1s<2s<2p<3s<3p<4s<3d<4p<5s<4d<5p<6s<4f<5d<6p<7s<5f<6d<7p<.......
1s বলতে বুঝায়, ১ম প্রধান শক্তিস্তরের s উপশক্তিস্তর।যেটাতে সর্বোচ্চ 2 টি ইলেক্ট্রন থাকে।অর্থাৎ 1 2 3 4... দ্বারা প্রধান শক্তি স্তর আর s p d f দ্বারা উপশক্তিস্তর বুঝাচ্ছে।এগুলোতে ক্রমানুসারে ইলেক্ট্রন বসিয়ে দিলেই যেকোন মৌলের ই. বিন্যাস হয়ে যাবে।
কি মনে হচ্ছে শক্তিক্রম মুখস্ত করতে দম বেরিয়ে যাবে।তাহলে তো হবে না, তোমাকে একদমেই মুখস্ত করতে হবে!!
চিত্রটি লক্ষ্য কর:

চিত্রে আমরা দেখতে পাচ্ছি, কেউ ডান থেকে একটি তীর মেরেছে।আর সেটা 1s কে ভেদ করেছে।আবার ২য় বার মেরেছে যেটা 2s কে ভেদ করেছে।৩য় বার 2p 3s কে ৪র্থ বার 3p 4s কে ৫ম বার 3d 4p 5s কে।----এভাবে মারছেই-----
এবার পর্যায়ক্রমে সাজিয়ে দেখ কি হয়?কি শক্তিক্রমের সাথে মিলে গেছে তো! চিত্রটা ভালভাবে লক্ষ্য করে চেষ্টা কর।হয়ে যাবে।
আশা করি তীর মেরে শক্তিক্রম ভেদ করতে পেরেছ। তোমরা অনেকেই ভাবছো পরীক্ষার খাতায় কিংবা mcq এর সময় ইলেক্ট্রন বিন্যাস করতে কি প্রত্যেকবার এটি আঁকিয়ে করা সম্ভব?হ্যাঁ ঠিকই বলেছো।তবুও বলব মুখস্ত করতে হবে না।শক্তিক্রমটি ভালভাবে দেখ এর মধ্যেও কিছুটা মিল তাল আছে।যেগুলো আমার চোখে ধরা পড়েছে তা লিখছি
*সিরিয়াল অনুসারে ধরলে s এরপর pএরপর d এরপরf হয়।কিন্তু তা হয় নি।
প্রত্যেকবার কিন্তু সিরিয়াল p উপশক্তিস্তরেই গিয়ে ভেঙেছে।যেটা শুরু হয়েছে 3p থেকে।তাই এরপর যখনই সিরিয়ালানুযায়ী 3p তে যাবে তখনই বুঝবে সিরিয়াল ভাঙা শুরু।
* p এর সিরিয়াল ভেঙে 4d এর আগ পর্যন্ত প্রত্যেকবার এরপর d না বসে এর জায়গায় পরবর্তী শক্তিস্তরের s ঢুকেছে।মানে 3p থাকলে এরপর 4s। 4p থাকলে এরপর 5s।s এর পরেই কাঙিখত 3d বা 4d বসেছে।
* 4d এর4 থেকে শুরু হয়ে শক্তিক্রম 4,5,6 4,5,6,7 5,6,7,8 এভাবে বসেছে।4d এর পর 4 থাকলে তা তো ক্রমানুযায়ী 4f হবে বা 5s এর পর 5 থাকলে তা যে ক্রমানূযায়ী 5p হবে এটা নিশ্চয়ই বুঝতে পারছো।এভাবে সাজিয়ে দেখ সব মিলে যাবে।
আশা করি শক্তিক্রম শিখে গেছো।এরপর যেকোন মৌলের কুরতে শুধু শক্তিক্রম গুলোতে প্রয়োজনীয় সংখ্যক ইলেক্ট্রন বসাও।তবে তা যেন সর্বোচ্চ মানকে অতিক্রম না করে।মানে p তে 14 টা ইলেক্ট্রন দিলেই কিন্তু বিপদ! এরপর দেখ প্রধান শক্তিস্তর 1 এ কয়টি, 2 এ কয়টি এককথায় কার কতটি যোগ করে প্রধান শক্তিস্ত লিখে ফেল।ব্যাস হয়ে গেল! উদাহরণ দেওয়া যাক
K(19)--1s
2 2s
22p
6 3s
23p
23d
0 4s
1
K(19)--2, 8, 8, 1
এখানে শক্তিক্রম গুলো ক্রমানূযায়ী না সাজালেও ইলেক্ট্রন কিন্তু অবশ্যই শক্তিক্রমানুসারে দিতে হবে।এটাই নিয়ম।এজন্য এখানে দেখ 3d তে 0 দিছি।কারণ, শক্তিক্রমানুসারে 3p এর পর 4s আসে যেখানে 1 টি ইলেক্ট্রন দিতেই পটাশিয়াম(K) এর 19 টি ইলেক্ট্রন পূর্ণ হয়ে গেল।
ব্যাতিক্রম: আমরা জানি ইলেক্ট্রনগুলি প্রবেশ করে 1s--2s--2p--3s--3p--4s--3d--.
......... এই নিয়মে।কিন্তু দেখা যায় p d f অরবিটাগুলি অর্ধপূর্ণ বা পূর্ণ থাকলে তা অধিকতর স্থায়ী হয় গঠন অর্জন করে।এজন্য s
2 d
4 না হয়ে s
1 d
5 হয়।কারণ এক্ষেত্রে d অর্ধপূর্ণ থাকে।একইভাবে d
9 s
2না হয়ে d
10 s
1 হয়।
এধরনের ইলেকট্রন বিন্যাস কেবল দু'টি মৌল ক্রোমিয়াম(
24Cr) ও কপার(
29Cu)।এদের ইলেক্ট্রন বিন্যাদ নিম্নরূপ:
Cr(24)-- 1s
2 2s
22p
6 3s
23p
63d
5 4s
1
Cr(24)--2, 8, 13, 1
Cu(29)-- 1s
2 2s
22p
6 3s
23p
63d
10 4s
1
Cu(29)-- 2, 8, 18, 1
বন্ধুরা তোমাদের কোন প্রশ্ন থাকলে কমেন্টে করতে পার।এজন্য কোন অ্যাকাউন্ট লাগবে না।আর ভাল লাগলে বিজ্ঞাপনে ক্লিক কর।সাথেই থাক।
কোনো পরমাণুতে ১ টি ইলেকট্রন থাকলে (H) সেটা কোন উপশক্তিস্তরে থাকবে তার কি কোনো নিশ্চয়তা আছে.....?? আর এক্ষেত্রে কোন শক্তিস্তরে থাকবে তার ও কি কোনো নিশ্চয়তা আছে....?? .... Kindly answer me fast.......
উত্তরমুছুন